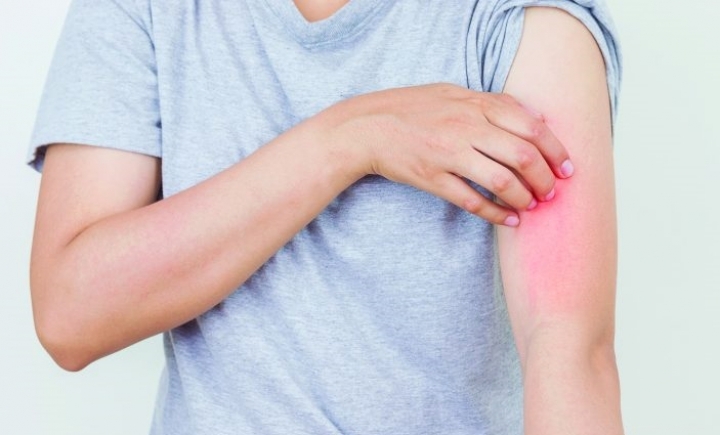
A LEO Pharma anunciou que a Food and Drug Administration (FDA) aprovou tralocinumab para o tratamento da dermatite atópica moderada a grave em adultos, maiores de 18 anos, nos casos em que a doença não esteja controlada com tratamentos tópicos ou nos casos em que estas terapêuticas não sejam aconselháveis.
“A aprovação de Tralocinumab pela FDA é muito importante para a LEO Pharma e para milhões de pessoas que vivem com dermatite atópica moderada a grave e que procuram conseguir uma opção de tratamento adequada para esta doença crónica e debilitante”, frisou o diretor financeiro e diretor executivo interino da LEO Pharma, Anders Kronborg.
A aprovação baseia-se nos resultados de segurança e eficácia dos ensaios clínicos pivotais de fase III ECZTRA 1, 2 e ECZTRA 3, que incluíram cerca de dois mil doentes adultos com dermatite atópica moderada a grave. Os dados de segurança foram avaliados a partir de um conjunto de cinco ensaios aleatorizados, com dupla ocultação controlados por placebo, incluindo os ensaios ECZTRA 1, 2 e ECZTRA 3, um ensaio de dose variável e um ensaio de resposta a vacinas.
“A dermatite atópica pode ser grave e imprevisível, pelo que o controlo da doença a longo prazo não é apenas um desafio para os doentes, mas também para os médicos que a diagnosticam e necessitam de prescrever um tratamento adequado, uma vez que as opções existentes para o tratamento desta doença crónica de pele são atualmente limitadas”, explicou o investigador dos ensaios clínicos de tralocinumab, Jonathan Silverberg.
Acrescentou que “este novo medicamento representa uma aquisição importante (…), enquanto tratamento desenvolvido para atuar e inibir especificamente a citocina IL-13, ajudando, assim, os doentes que vivem com dermatite atópica a terem controlo sobre a doença.”
O medicamento estará disponível em seringas pré-cheias de 150 mg/ml cada, para injeção subcutânea com uma dose inicial de 600mg, seguida de 300mg de duas em duas semanas. O medicamento pode ser usado com ou sem corticosteroides tópicos.
A aprovação pela FDA representa a quinta aprovação regulamentar global para tralocinumab em 2021.